染料废水处理技术详细介绍
今天为广大朋友介绍的是——染料废水处理技术 近年来,水污染日益严重,而目前传统的水处理方法难以处理水体中难降解的有机物(如染料和药物等)。因此,越来越多的学者研究了许多新方法来解决难降解有机物造成的水污染问题。染料在染色、涂料、颜料和纺织等领域被广泛使用,是造成水污染的一大原因。染料的化学结构复杂、有生物毒性且难于用传统的方法降解。亚甲基蓝(methylene blue , MB )作为一种偶氮染料在印染和纺织工业中应用广泛,因而被广泛的研究。 高级氧化技术(advanced oxidation processes , AOPs)作为难降解有机废水的一种有效的处理方法,近年来受到越来越多的关注。 AOPs是一种基于轻基自由基(·OH)氧化的技术,·OH具有仅次于氟的氧化势(2. 80 eV ),几乎可以无选择性氧化所有有机物,直至将有机物矿化成H2O,CO2和无机盐。目前,研究比较广泛的AOPs有光催化、 Fenton、光催化臭氧化、等离子体等,以及它们的协同技术。 等离子体尤其是低温等离子体技术,能原位产生·OH、H2O2、O3 、HO2·和·O等高能电子等活性物质,同时伴随着液电空穴、冲击波和紫外光辐射等物理效应。该技术是集多种AOPs的优点于一身的高级氧化技术。介质阻挡放电(dielectric barrier discharge , DBD)等离子体是低温等离子体的一种,具有电子密度高、放电均匀稳定等特点,受到广泛的重视。DBD反应器是在放电空间中插入绝缘介质的放电反应器,主要有板一板式和线一环式2种形式。阻挡介质即可以覆盖在电极表面,也可悬挂于放电空间中,形成电子密度较高的、均匀稳定的放电。 采用新型的双气室DBD等离子体反应器降解MB溶液,与传统板一板式DBD放电反应器相比,新设计的反应器增加了曝气,同时增加了一个气室。当两电极之间施加高压电时,放电在上、下气室同时发生,活性物质在两个气室和溶液中产生。产生的活性物质可以同时处理液层上下两个表面的有机物,同时由于曝气的作用,下气室产生的气体(主要是臭氧、含氮的氧化物)必须要经过溶液才能离开反应器,增加了活性气体在溶液中的停留时间,同时加强了气液相传质。本文研究了在新型双室DBD等离子体反应器中,液体体积、下气室高度、输入功率、初始pH、初始浓度和曝气种类对亚甲基蓝降解效率和溶液COD的影响。同时分析了MB的降解产物,初步提出了MB的降解机理。 一,实验部分 1. 1实验装置 实验采用图1所示的石英DBD反应器,外径140mm,内径134 mm,高度100 mm,底板厚2 mm,内部有4个长度为15 mm直径为6 mm的石英柱8固定在反应器内壁用来支撑曝气板。反应器壁上有2个石英制成的进气管3,实验气体(空气,O2)由2个进气管进入反应器。
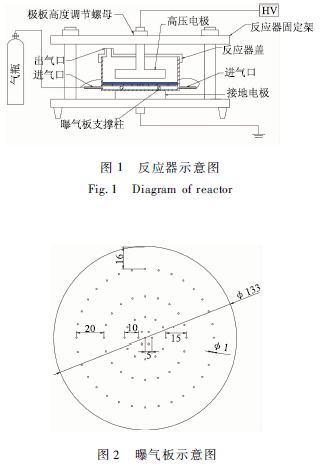
O2作为工作气体时,通气后加入溶液,盖好盖子后持续通气,用气相色谱分析出气日处气体,直至检测不到N2(30 min)再开始放电反应。反应空间用有机玻璃制成的盖子与外界分离。电极是由两块直径90 mm的不锈钢板制成,两电极分别与交流电源(15 kV/100 V)连接。与传统的平板DBD反应器不同的是在设计的反应器中液体不直接与接地电极表面的阻挡介质接触而是用一块如图2所示的多孔的有机玻璃板将溶液与接地电极分离。实验时先通入气体,然后再注入待处理溶液,盖上盖子,形成上下两个气室,电极间距用支架上的螺母调节。 传统的板一板式DBD反应器只具有一个放电空间,自然封闭的空气放电,无气体流动,等离子体产生的活性物质由于传质阻力无法到达液相主体,尤其是短寿命的自由基至多只能到达液层以下2 mm处。因此,传统DBD反应器只能处理液体表层的有机物,受扩散影响很大。与传统板一板式DBD放电反应器相比,新设计的反应器增加了曝气,同时增加了一个气室。当两电极之间施加高压电时,放电在上、下气室同时发生,活性物质在两个气室和溶液中产生。产生的活性物质可以同时处理液层上下2个表面的有机物,同时由于曝气的作用,下气室产生的气体必须要经过溶液才能离开反应器,增加了活性气体在溶液中的停留时间,同时加强了气液相传质。 1. 2试剂、仪器及分析方法 1. 2. 1实验试剂 亚甲基蓝(BS,科密欧),HR S04 ( AR,江天),NaOH ( AR,光复),重铬酸钾(AR,光复),硫酸亚铁钱(AR,光复),硫酸银(AR,光复),邻菲锣琳(AR,光复),Nat S04 ( AR,光复)。 1.2.2实验仪器 紫外可见分光光度计(LS S,上海仪电分析仪器有限公司),pH计(pHS-3 C,雷磁),电导率仪(DDS-11C,雷磁),质量流量控制器( D07-7A/ZMM,北京建中机器厂),流量显示仪(D08-4C/ZM,北京建中机器厂),电子天平(AL204,梅特勒一托利多仪器有限公司),高压变压器(15 kV/100 V,50 Hz,青县同科电器制造有限公司),气相色谱质谱联用仪(CCMS) ( Agilent 5977A MSD, Agilent 7890B CC System, Agilent Teoh-nologies ),液相色谱质谱联用仪(LCMS) ( LCQ Deoa XP MAX, Thermo Fisher) 。 1.2.3分析方法 用电子天平称取0. 1 g的MB固体用去离子水定容到100 mL,制成浓度为1 g / L的MB储备溶液,根据实验需要,分别稀释成浓度为50 、 100和200 mg / L 的MB实验溶液,实验为间歇操作。采用紫外可见分光光度法与采用高效液相色谱法都可以准确的表示MB的浓度变化。本实验采用紫外可见分光光度法测量MB的浓度,由标准曲线可知MB的浓度在10 mg / L以下符合朗伯一比尔定律,因此每次测量都取出1 mL的溶液稀释相应的倍数,在比较大吸收波长664 nm下测量吸光度,MB的脱色率DE用(1)式计算。空气曝气时取样间隔20 min,氧气曝气取样间隔5 min。有机物的矿化用COD的脱除率间接测量。COD采用重铬酸盐法测量(GB 11914-89 ) , COD脱除率ME用式(2)计算。降解MB的能量效率Y用(3)计算。pH用稀硫酸H2SO4(0.2 mol / L)和NaOH溶液(0. 2 mol / L)调节。氧气DBD等离子体处理15 min后的产物用CCMS和LCMS分析。
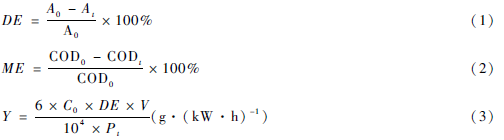
式中:A0为溶液的初始吸光度;A为处理时间为t时溶液的吸光度;V为处理液体的体积(mL);P为输入功率(w);t为处理时间(min ) ; C0为溶液的初始浓度(mg /L) ;COD0为初始化学需氧量(mg /L'),CODt为处理时间为t时的化学需氧量(mg /L)。 二,结果与分析 2. 1处理液体积(液层厚度)对MB降解的影响 实验采用初始浓度为50 mg /L、初始pH为4. 0、初始电导率为84 μS /cm的MB溶液,空气流量60 SCCM,输入电压6 kV,输入功率18 W,高压电极与液面间距(上气室高度)7. 5 mm,下气室高度7 mm处理液体积对脱色率和能量效率的影响如图3所示,随处理液体的体积增加MB的脱色率下降,但能量效率却升高。 液层的厚度随处理液体的体积增加而增加,等离子体中的短寿命活性物质尤其是·OH(3.7 x 10-9 s)只能到达液体表面,未能与液体内部有机物充分接触,导致MB的脱色率较低。但对于较多的溶液,由于溶液中含有的MB分子数量较多,溶液浓度随时间变化较慢,MB分子与放电空间中产生的活性物质发生碰撞的机会较大,能量效率较高。但体积多的溶液中MB分子的数量较多,虽然能量效率有所提高(即溶液中MB分子降解的绝对量增加),但溶液多时MB分子的总数也多,因此,MB溶液的脱色率却下降。 Y随降解时间的增加达到比较大值后下降,处理50 mL溶液时,能量效率在40 min时达到比较大值,而处理100 mL溶液时,能量效率在80 min时达到比较大。在少量的溶液中,MB分子可以在较短的时间内被降解,随溶液中MB浓度下降,中间产物的浓度增加,等离子体产生的活性物质与MB碰撞、反应的机率降低,因此能量效率下降较快。而溶液较多时,浓度变化较慢,随放电时间增加溶液中MB的浓度下降,中间产物的浓度升高,达到一定值时,能量效率也随即下降(80 min )。为了获得较高的脱色率,本文选择溶液的体积为50 mL。
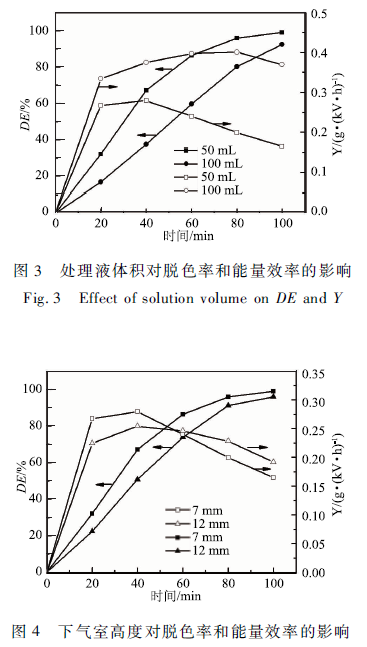
2. 2下气室高度对MB降解的影响 实验采用初始浓度为50 mg / L 、体积50 mL、初始pH为4. 0,初始电导率为84 μS /cm的MB溶液,空气流量60 SCCM,输入电压6 kV。为了保证稳定放电,上气室高度固定7. 5 mm。研究下气室高度分别为7 mm , 12mm对MB的脱色率和能量效率的影响。由图4可知,随下气室高度增加MB的脱色率下降,但能量效率先下降后升高。 一方面,电极间距加大,放电空间内的电场强度下降,在输入电压相同的条件下,下气室高度从7 mm增加到12 mm,输入功率从18 W下降到15 W。输入电能减少,使放电空间中活性物质减少,导致脱色率和能量效率下降。 另一方面,电极间距增大使更多能量用于形成等离子体隧道。电极间距较大时,等离子体隧道较长,随放电时间增加,反应空间内温度和浓度梯度增大,导致活性物质(自由基、激发态分子、原子)在放电空间内重新组合、淬灭。活性物质在反应空间内的重新组合虽然可以增强物理效应(紫外光的强度),但非平衡等离子体对有机物的降解作用主要是化学效应的作用,过多的物理效应对MB溶液的降解起不到明显的作用。因此,电极间距较大的反应器中MB的脱色率较低。但随反应进行,放电空间内MB的浓度降低,虽然电极间距较小时,放电产生的活性物质的浓度较高,但此时MB的浓度较低,与活性物质碰撞反应的几率下降,此时下气室高度不同导致的脱色率的差别减小。而输入电压相同时,电极间距较大的反应器的输入功率较低,由式(3)可知,在脱色率差别较小时,输入功率下降将导致能量效率升高。因此,在反应后期电极间距较大的反应器的输入功率较小使能量效率的计算值较高。 另外,随着反应进行,溶液的电导率从初始的84 μS /cm升高到3. 01 mS / cm ( DBD处理100min,电导率的升高使电场强度进一步下降、等离子体隧道难于形成、活性物质的浓度也进一步下降。由于电极间距较小的反应器中电场强度、活性物质的浓度较高,电导率上升导致的削弱作用较明显,此时由活性物质浓度下降导致的MB的脱色率下降和输入功率较大共同导致能量效率计算值急剧下降,此时(放电60 min后),电极间距较小的反应器的能量效率计算值小于电极间距较大的反应器。在放电前60 min,下气室高度为7 mm的反应器中MB的脱色率和能量效率都较高,且MB脱色率在下气室高度为7 mm的反应器中一直较高。因此,选择下气室高度为7 mm。在HU等用等离子体降解果乐的研究中,也得到了相似的结果,果乐的降解率随电极间距的增加而下降。 2. 3输入功率对MB降解的影响 实验采用初始浓度为50 mg / L 、体积50 mL、初始pH为4. 0、初始电导率为84 μS /cm 的MB溶液,空气流量60 SCCM,上、下气室高度分别为7. 5和7mm。通过改变输入电压5,6和7 kV,输入功率分别为12.5 ,18和24. 5 W。如图5所示,随着输入功率的增加,MB的脱色率增加,但能量效率下降。虽然增加能量的输入有利于MB的快速降解,但能量耗散的也较多。这是由于输入功率增加,容易产生火花放电,更多的能量用于产生热量,导致溶液温度上升。同时温度上升会加快自由基的淬灭,使能量效率下降。因此,输入功率的选择需要权衡降解速率和能量效率。由图7可知,放电处理60min时,输入功率从12. 5 W提升到18 W MB的脱色率从77. 2%提升到86.5 %,输入功率从18 W提高到24. 5 W脱色率仅提升到87.2%,但能量效率却从0.24 g / (kW · h)下降到0.18 g / (kW · h)。因此,选择输入电压6 kV,输入功率为18 W可以合理地利用能量的同时获得较高的降解率。


2. 4 pH对MB降解的影响 实验采用初始浓度为50 mg/L、体积50 mL的MB溶液,空气流量60 SCCM,上气室高度7. 5 mm,下气室高度7 mm,输入电压6 kV。改变初始pH分别为4.0,7.0和10. 0。在图6中可以看出pH=4.0和pH = 10. 0时MB的脱色率和能量效率都较高,pH =4. 0的脱色率比较高。这是因为在本实验中臭氧起到重要的降解作用,在酸性条件下臭氧的浓度较高主要发生臭氧的直接氧化反应,在碱性条件下主要发生通过轻基自由基(·OH)降解MB的间接氧化反应,而中性条件下,臭氧液相中的浓度较低。除此而外,pH会影响MB分子在水中的状态,解离的浓度不同也会导致速率常数的差别。综合以上因索,酸性和碱性条件下MB的降解率和能量效率都较高,pH为4. 0时降解效果比较好,选择pH 4. 0为实验条件。 2. 5初始浓度对MB降解的影响 实验采用50 mL初始pH为4. 0,初始浓度分别为50,100和200 mg/L ,电导率分别为84,150和200 μS /cm的MB溶液,空气流量60 SCCM,上、下气室高度分别为7. 5和7 mm,输入电压6 kV。如图7所示,MB的脱色率随初始浓度的增加而下降,而能量效率随初始浓度的增加而升高。 一方面,随初始浓度的增加,MB降解产生的中间产物的浓度增加。MB与中间产物都和等离子体产生的活性物质反应,但在相同的输入功率下活性物质的浓度为定值,因此在高浓度的MB溶液中,脱色率较低,但由于高浓度的MB溶液中MB分子的数量较多,有更多的机会与活性物质发生作用,因此高浓度的溶液的能量效率较高。另一方面,随着溶液浓度的增加溶液的透光性变差,降低了紫外光对溶液的作用,也是导致脱色率下降的另一原因。MACUREANU等在用DBD反应器降解己酮可可碱(pentoxifylline)的研究中也得到了相似的结果。

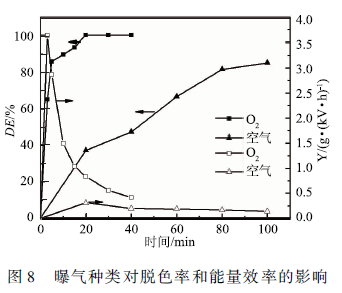
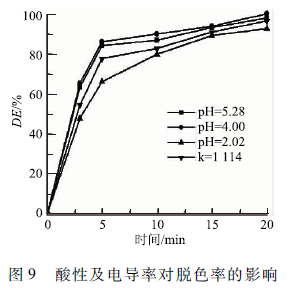
2. 6曝气种类对MB降解的影响 实验采用初始浓度为100 mg/L,体积50 mL,初始pH为4. 0,电导率为150 μS /cm的MB溶液,分别采用空气、O2曝气,气体流量60 SCCM,上、下气室高度分别为7. 5和7 mm,输入电压6 kV。如图8所示,氧气可以在20 min内使MB的脱色率达到99. 98 %,而空气需要100 min才能将MB脱色85.3 %。氧气曝气时,处理3min能量效率比较高,比较高可达3.63 g / (kW · h),而空气曝气时比较大能量效率在20 min时达到比较大,比较大能量效率为0. 31 g / (kW · h)。 一方面,由于反应器的电极间距较大,放电间距存在大量气体,空气中79% ( V/V)为N2 , N2的键能(9. 8 eV)大于O2(5.2 eV),解离N2要消耗比解离O2更多的能量。另一方面,从图8可以看出,O2曝气的能量效率比空气曝气的能量效率大一个数量级,这不仅仅是因为在空气中解离N2要消耗较多的能量,更主要的原因是在空气中大量的N2解离后与激发态的O反应,产生NOx(主要是NO和NO2 )。这一方面消耗了空气系统中的氧气,使O3等含氧活性物质的浓度下降,另一方面产生的NO·和NO2·在酸性条件下与·OH反应,产生过氧亚硝酸(HONOO) 。虽然过氧亚硝酸也有较高的氧化势(2. 4 eV) ,但是由于过氧亚硝酸的形成消耗了氧化势更高的·OH(2.80 eV),且HONOO容易异构成硝酸而失去强氧化能力,且导致酸性效应和电导率升高。 从2. 4的研究中可知酸性pH下MB的脱色率和能量效率都较高。为了进一步研究酸性的增加对MB降解的促进作用和NO的产生导致的反应中毒(含氧活性物质浓度的下降、电导率的升高)对MB的影响。在氧气条件下,处理初始浓度为100 mg/L的MB溶液,分别调节MB溶液的pH为2. 02(空气处理100 min时的pH为2. 07 ) 、4. 00和5. 28(不加硫酸的MB溶液的pH ),在pH为4. 00的溶液中加入硫酸钠调节初始电导率(k)至1 114 μS / cm ,得到图9。酸性增强对MB降解并不总是有利的,在pH从5. 28下降到4. 0时,MB的脱色率增加,但是当pH进一步下降到2. 02时,溶液的脱色率显著下降。pH为5.28、4. 00和2. 02时溶液的电导率分别为64 、 150和4. 08 mS / cm 。强酸性条件不利于MB的降解,是由于电导率升高导致电场强度下降,等离子体隧道难于形成,活性物质浓度下降,从而导致的MB的脱色率在强酸性条件下较低。电导率升高导致的MB降解抑制效应,在加入硫酸钠调节初始pH为4. 0的MB溶液的电导率k=1 114 μS / cm 降解MB溶液的实验中,得到脱色率下降的结果中得到进一步的证实。因此,酸性的增强对MB降解的促进作用与酸性增强导致的电导率升高对MB降解的抑制作用相比较弱。因此,空气曝气时NOx的产生,导致的酸性效应并不能加强MB的降解,NOx的产生导致的反应中毒(氧化性物种中毒以及电导率升高等)是使MB的降解效率下降另一重要原因。
由于实验采用的反应器有两个气室,气体流速较低,放电产生的气体在反应器中停留时间较长,因此,在空气曝气时反应中毒现象更加明显。为避免氧化物中毒,采用O2曝气,放电产生的含氧活性物质在反应器内也会累积,从而使脱色率和能量效率都有所提高。综上所述,新设计的双室DBD反应器不仅会加强氧气放电的化学效应,增强氧化性物种的停留时间,同时也使空气放电时反应中毒现象更加明显。在DBD等离子体与活性炭协同降解五氯酚的实验中,在1. 5 h等离子体处理后,在氧气和空气条件下的五氯酚的降解率分别为85%和78%。在新设计的双室DBD反应器中,20 min的等离子体处理后,在氧气和空气条件下的MB的降解率分别为99. 98%和37. 39%。氧气曝气3 min时能量效率比较高,比较高能量效率可达3. 63 g / (kW · h) 。 HUANC等采用传统的DBD,在pH为5. 68时处理40 min, MB溶液降解率达99. 79 % 。JI等用LiFe ( W04 ) 2作非均相Fenton试剂降解MB,在催化剂浓度10 g / L,过氧化氢浓度40 mmol /L , pH5.0,50 ℃时,200 mg/L的MB溶液处理100 min后降解率可以达到接近100% 。 KERKEZ等用负载Ag2O的TiO2在初始pH为5,可见光的条件下光催化处理MB溶液180 min,降解率比较高可达48. 90 %。但光催化、非均相Fenton反应都需要外加试剂,存在后续分离麻烦、处理成本高以及降解效果差等问题。双室DBD反应器与传统的平板DBD反应器相比,虽然在空气曝气时效率有所下降,但在氧气曝气时具有较高的能量效率,且不需要额外添加任何试剂。综上所述,新型双室DBD等离子体反应器在氧气曝气的条件下表现出突出的优势,能以较高的能量效率有效的降解MB溶液。 2. 7不同曝气种类对MB矿化的影响 实验采用初始浓度为100 mg/L,体积50 mL,初始pH为4. 0,电导率为150 μS / cm的MB溶液,分别采用空气、O2曝气,气体流量60 SCCM,上、下气室高度分别为7. 5和7mm,输入电压6 kV。考察分别在空气和O2的气氛条件下,ME随时间的变化,结果如图10所示。在空气曝气100 min后COD脱除率仅达到54. 61 %,而O2曝气40 min后COD脱除率就可以达到69. 78%。反应体系中O2曝气可以产生大量的O3、H2O2和·OH等含氧活性物质。尤其是O3,在氧气曝气时,在放电作用下,下气室中O3的浓度较高,相当于一个臭氧发生器,与上气室的液相表面放电等离子体发生协同作用;同时,下气室的气体离开反应器一定要经过MB溶液,因此U3在液相中的的停留时间增加,使COD的脱除率提高。但在空气曝气条件下,放电产生大量的NOx(主要是NO和NO2)积聚在下气室,与产生的含氧活性物质(主要是·O,·OH,H2O2和O3)反应,此外,NOx的形成消耗了系统中的氧减少了系统中含氧活性物质的浓度,由于含氧活性物质比NOx更能有效的降解MB分子。因此,在空气曝气时,降解和矿化效果较差。

与图8中的DE随时间的变化曲线对比可知,MB的矿化比降解要慢许多。这是由于MB经过一系列的复杂的反应,生成许多有机中间体,由于MB分子相对容易被氧化,而生成的有机中间体比MB分子结构更加稳定,这些中间体与反应系统中的活性物质反应被降解的难度加大。因此,反应物系中有机物的矿化比MB的脱色更加困难,矿化速率相对较慢。 2. 8 MB降解产物及机理分析 氧气等离子体处理MB溶液15 min后,得到的溶液用GCMS和LCMS分析,检测到的中间产物如图11和12所示。根据已有研究和前面结果推断,MB分子的降解主要通过3种途径:高能电子攻击、臭氧氧化和轻基化。
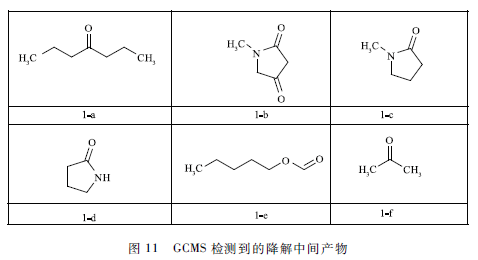
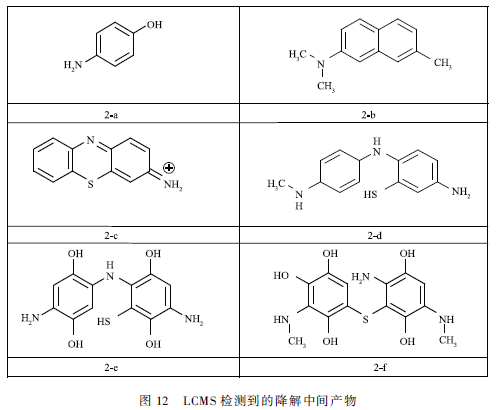
通过电子攻击不断的脱甲基,随后开环,MB分子从杂环化合物先降解为芳香化合物再开环成为脂肪化合物,直至比较终矿化。产物2-c主要是电子攻击MB,导致MB分子脱甲基化形成的产物。轻基自由基攻击则是·OH不断攻击芳环,MB分子从复杂的杂环化合物先分解为脂肪化合物再降解为更小的分子,比较终矿化。产物2 -e和2 -f主要是由MB分子轻基化形成的。臭氧直接氧化,主要路线是通过Criegee机理,O3攻击有机物的不饱和键形成三氧环状中间体,随后三氧环状中间体分解成碳基化合物(竣酸、醛和酮)和CO2,但形成的有机酸、酮和醛难于通过臭氧直接矿化。GCMS检测到的图11中的产物主要是由O3直接氧化产生的。综上所述,我们认为MB的降解是脱甲基化、轻基化和臭氧氧化协同作用的结果。 三,结论 本研究采用一种新型的双室DBD反应器对MB溶液进行降解,MB的脱色率随处理液体积增加,初始浓度的增加,下气室高度的增加,输入功率的减小而下降。在弱酸性和碱性条件下MB的脱色率较高。DBD等离子体处理20 min时,O2的脱色率是空气的4. 4倍,在MB初始浓度为100 mg / L ,体积50 mL,初始pH为4. 0,电导率为150 μS / cm,O2流量60 SCCM,上、下气室高度分别为7. 5和7 mm,输入电压6 kV(输入功率18 W)时,处理20 min后,MB几乎脱色完全(99. 98 % )。放电40 min后COD脱除率可达69. 78 %,能量效率比较高(3 min )可达3. 63 g / (kW · h)。反应器在空气和氧气作为工作气体时,双室DBD等离子体反应器对MB的降解效果差别很大,在新设计的反应器中空气放电的缺点(生成NOx导致反应中毒)和氧气放电的优点(含氧活性物质浓度较高)都被加强了。通过对比,光催化、Fenton反应、传统平板DBD放电反应器,新设计的双室DBD反应器在氧气为工作气体时具有较大的优势。同时,通过分析MB的降解产物,提出MB的降解是脱甲基化、轻基化、臭氧氧化协同作用的结果。

污水处理设备联系方式: 销售热线:010-8022-5898 手机号码:186-1009-4262 (责任编辑:李德馨) |